O modelo de Thomson
 |
|
O modelo de Dalton
possibilitou explicação de diversos fenômenos e contribuiu muito para a
evolução do conhecimento da matéria. No entanto, não considerava a
natureza elétrica da matéria.
A eletricidade era estudada desde o
século XVIII, e os cientistas avançavam em novas pesquisas e
experimentos. A teoria referente à existência de uma partícula da
matéria de carga negativa, o elétron, se consolidava.
Novos conhecimentos, novas questões
eram formuladas, e o modelo de Dalton não satisfazia, pois não
explicava a existência do elétron. Era necessário, então, um modelo que
tivesse como base o fato de a matéria, portanto o átomo, possuir
partículas com a carga elétrica negativa e, supostamente, também conter
partículas com carga elétrica positiva.
|
Cerca de um século depois de Dalton, o cientista inglês Joseph John Thomson propôs outro modelo para explicar o átomo, levando em consideração o conhecimento já existente sobre eletricidade.
Em 1887, Thomson afirmou que o
átomo seria uma esfera neutra, maciça e não-homogênia, composta por um
fluído positivo onde estariam dispersos os elétrons.
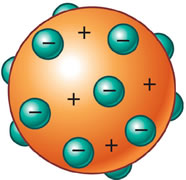
No modelo de Thomson, o átomo continua sendo representado por uma minúscula esfera maciça, porém revela o átomo como uma estrutura complexa e divisível.
Esse modelo de átomo á chamado por alguns de “pudim de passas”: a massa do pudim seria a carga positiva, e as passas espalhadas sobre o pudim seriam as partículas negativas – os elétrons.
A descoberta e os estudos de
radioatividade, além dos significativos avanços tecnológicos, levaram os
cientistas a novas especulações sobre a composição da matéria e a
estrutura do átomo.
O Modelo de Rutherford
Em 1904, o cientista neozelandês Ernest
Rutherford realizou um experimento que ficou conhecido na história da
ciência como experimento de Rutherford. Ele já sabia da existência das
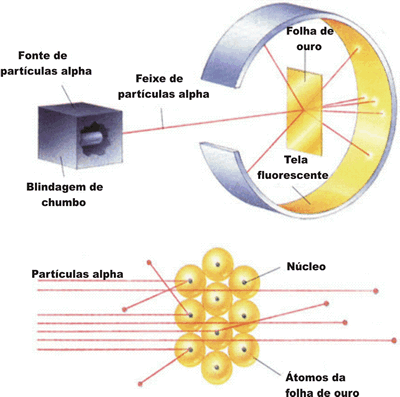
partículas de carga positiva, denominadas partículas alfa ( 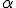 ). Em seu experimento, Rutherford colocou no interior de um bloco de chumbo uma substância emissora de partículas 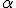 , de forma que elas fossem orientadas, por meio de um orifício em uma placa de chumbo, a colidir contra uma fina lâmina de ouro.
Observe o esquema do experimento de Rutherford:
Com esse experimento, ele verificou que:
Analisando esses resultados, Rutherford concluiu que:
-
O átomo não é uma esfera maciça. Existem grandes espaços vazios visto que a maior parte das partículas 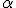 atravessou a lâmina de ouro.
-
O átomo possui uma região central onde
está concentrada a sua massa. Foi contra essa região, denominada por ele
de núcleo, que as partículas 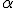 , se chocaram e retornaram.
-
Esse núcleo apresenta carga positiva, pois repeliu a partícula 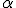 - que também possui carga positiva.
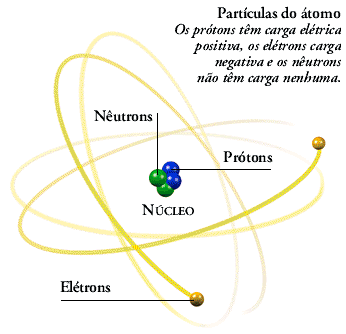
Com esses dados, Rutherford construiu um
modelo atômico semelhante ao Sistema Solar, em que o átomo é uma
partícula muitíssimo pequena composta de duas regiões:
- uma interna, o núcleo, onde estariam concentradas
praticamente toda a massa do átomo – de carga elétrica positiva,
representada por partículas chamadas de prótons;
- outra externa, de massa desprezível, onde estariam os elétrons, diminutas partículas negativas em movimento ao redor do núcleo.
Nos modelos aqui apresentados, as
dimensões do núcleo e da eletrosfera não estão em escala. Na realidade, a
eletrosfera tem o seu volume cerca de 100 mil vezes maior que o do
núcleo.
Em 1932, o físico inglês James Chadwick
(1891-1974), realizando experiências com material radioativo, comprovou
uma das hipóteses de Rutherford que afirmava a possibilidade de existir
no núcleo uma outra partícula desprovida de carga elétrica.
Chadwick chamou essas partículas de nêutrons.
O modelo de Rutherford-Böhr
O modelo atômico de Rutherford foi complementado com um novo conceito introduzido pelo físico dinamarquês Niels Bohr:
“O elétrons descreve uma órbita circular ao redor do núcleo sem ganhar ou perder energia.”
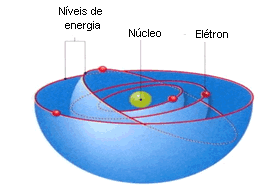
Cada órbita descrita pelo elétron é
denominada nível de energia ou camada de energia. Em um átomo, há várias
órbitas circulares, cada uma delas com um determinado valor energético.
Outros modelos que vieram depois
especificam as características das órbitas ou camadas de energia,
incorporando a discussão de elétron considerado como partícula e/ou
onda.
Pesquisas mais recentes, realizadas após a
elaboração do modelo de Rutherford-Böhr, comprovaram que impossível
determinar num mesmo instante a posição e a velocidade de um elétron.
Por isso, cientistas afirmam que existe a probabilidade de os elétrons
estarem em uma ou outra região da eletrosfera.
O Interior do Átomo
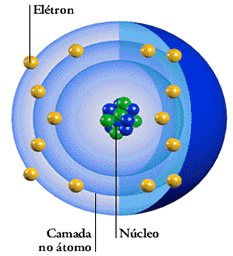
No centro de um átomo está o seu núcleo,
que apesar de pequeno, contém quase toda a massa do átomo. Os prótons e
os nêutrons são as partículas nele encontradas, cada um com uma massa
atômica unitária.
O Número de prótons no núcleo estabelece o
número atômico do elemento químico e, o número de prótons somado ao
número de nêutrons é o número de massa atômica. Os elétrons ficam fora
do núcleo e tem pequena massa.
Características das Partículas:
- Prótons: tem carga elétrica positiva e uma massa unitária.
- Nêutrons: não tem carga elétrica, mas tem massa unitária.
- Elétrons: tem carga elétrica negativa e quase não possuem massa.
Cargas elétricas e massas
Inúmeros experimentos realizados
permitiram estabelecer as propriedades das partículas do átomo quanto à
sua carga elétrica e massa.
Quando à carga elétrica: considera-se a carga do próton igual a +1; a carga do elétron igual a -1, e a carga do nêutron igual a 0.
Como se sabe, cargas elétricas de mesma
intensidade e de sinais contrários se neutralizam. Ou seja, a carga
elétrica de um próton (positiva) anula a carga elétrica de um elétron
(negativa). Qualquer átomo apresenta número de prótons e de elétrons
iguais; logo, é eletricamente neutro.
Quanto a massa: tendo o
valor da massa do próton como referência, afirma-se que a massa do
nêutron é praticamente igual à massa do próton. Como o próton possui
massa cerca de 2 mil vezes maior que a de um elétron, esta última é
considerada desprezível.
O núcleo do átomo
Agora, vamos considerar melhor as características do núcleo atômico.
Número atômico
Há muitos átomos diferentes entre si. Por
exemplo, o átomo de alumínio é diferente do átomo de ouro. Qual será a
principal diferença entre os tipos de átomos?
Após estudos definiu-se que o número de prótons é uma das principais características que diferenciam um átomo do outro.
Esse número é chamado de número atômico e é representado pela letra Z.
- Z é a “carteira de identidade” do átomo, pois indica a qual elemento químico cada átomo pertence.
- O conjunto dos átomos que possuem o mesmo número atômico (Z) é denominado elemento químico.
Portanto, a partir do conceito de
elemento químico, á possível afirmar que átomos com número de prótons
diferentes entre si pertencem, obrigatoriamente a elementos químicos
diferentes. Vejamos:
O átomo de sódio tem 11 prótons; logo,
seu número atômico é igual a 11 (Z = 11), e todos os átomos com número
atômico (Z) igual a 11 pertencem ao elemento químico sódio.
Número de massa
É a soma do número de prótons com o número de nêutrons. O número de massa é representado pela letra A.
Nesta expressão, temos: A = número de massa;
p = número de prótons;
n = número de nêutrons.
Logo, a diferença entre o número de massa e o número atômico revela o número de nêutrons.
A soma do número de prótons com o número
de nêutrons, ou seja, o número de massa (A), não corresponde a toda a
massa do átomo, pois também existem os elétrons. O motivo de A
representar a massa do átomo é que a amassa do elétron é desprezível
quando comparada com a dos prótons e nêutrons.
Átomos pertencentes ao mesmo elemento
químico podem apresentar diferentes números de nêutrons. A prata, por
exemplo, é encontrada na natureza com números de nêutrons distintos: 60 e
62. Se somarmos esses números com o número de prótons, que é igual a
47, teremos:
- 60 nêutrons + 47 prótons = 107 como número de massa.
- 62 nêutrons + 47 prótons = 109 como número de massa.
Por isso, somente o número atômico pode identificar a que elemento químico o átomo pertence.
Representação dos átomos
Os átomos dos elementos químicos são representados por símbolos composto por uma, duas ou três letras. Para o sódio, utiliza-se Na, para o cloro Cl; para o carbono, C; e assim por diante.
Note que a primeira letra é sempre maiúscula. Normalmente, o número de massa (A) é representado no canto superior esquerdo, e o número atômico (Z) no canto inferior esquerdo.
Observe o exemplo para o elemento químico cloro:
Semelhanças atômicas
Além da existência de vários átomos com o
mesmo número de prótons, pesquisas indicam que semelhanças podem
ocorrer também com o número de nêutrons e com o número de massa.
Os átomos que possuem algum tipo de semelhança são agrupados em três grupos básicos: isótopos, isótonos e isóbaros.
Átomos isótopos
são aqueles que apresentam o mesmo número de prótons e diferente número
de nêutrons e de massa. Obrigatoriamente, pertencem ao mesmo elemento
químico.
Exemplo:
Átomos isótonos
são aqueles que apresentam o mesmo número de nêutrons e diferente
número de prótons e de massa. Obrigatoriamente, não podem pertencer ao
mesmo elemento químico.
Átomos isóbaros
são aqueles que apresentam o mesmo número de massa e diferente número
de prótons e de nêutrons. Obrigatoriamente, não podem pertencer ao mesmo
elemento químico.
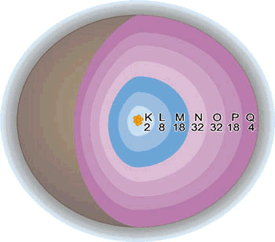
Eletrosfera e níveis energéticos
 |
|
Como vimos anteriormente, Bohr aperfeiçoou o modelo atômico de Rutherford com base em formulações teóricas. Uma delas é esta:
Os elétrons estão
distribuídos de acordo com suas distâncias em relação ao núcleo,
descrevendo órbitas circulares ao redor deste sem ganhar ou perder
energia.
Assim, há várias órbitas circulares
em um átomo, e cada uma delas tem um determinado valor energético.
Dependendo do número de elétrons que possui, o átomo pode apresentar
vários níveis eletrônicos ou camadas de energia.
Esses níveis eletrônicos, conforme o número de elementos químicos conhecidos, são numerados de 1 a 7 ou representados pelas letras K, L, M, N, O, P e Q, a partir do nível mais interno, que é o mais próximo do núcleo.
|
Bohr afirmou também que:
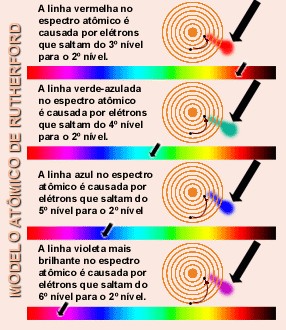
Ao receber energia o
elétron pode saltar da camada em que está para uma camada mais externa;
quando cessa a fonte de energia, ela retorna para a camada de origem,
liberando sob a forma de luz a energia anteriormente recebida.
Pela observação das fotos seguir, você verá que a chama apresenta cores diferentes.
O que se pode constatar ao observar as diferentes cores apresentadas nas fotos?
Isso ocorre porque os elétrons dos
diferentes elementos químicos atingem camadas externas também diferentes
ao ganhar energia. A emissão da luz depende da diferença de energia
entre a camada eletrônica em que o se encontrava e a camada para a qual
“saltou” ao receber energia.
A energia em forma de
luz é emitida quando o elétron retorna à sua camada eletrônica inicial,
e a cor da luz dependerá de cada elemento químico.
Como a luz visível é formada por
ondas eletromagnéticas distribuídas numa certa faixa de frequências, e a
frequências da onda corresponde a quantidade de energia que ela
transporta, temos que, a energia emitida pelo elétron é percebida por
nós na forma de luz com a cor determinada pela quantidade de energia
liberada.
Isso explica, por exemplo, as cores
dos fogos de artifício, já que eles são produzidos com adição de
substâncias que emitem luz quando aquecidas.
Como vimos, de acordo com a teoria
de Bohr, ao receber energia um elétron pode saltar para uma camada mais
externa, de maior energia.
Atualmente, sabemos que, se a
quantidade de energia fornecida a um elétron for muito elevada, esse
elétron poderá saltar para fora da área considerada eletrosfera. Em
conseqüência, o átomo deixa de apresentar igual número de prótons e
elétrons, deixando, portanto de ser neutro.
|
|
 |
Da mesma forma que se podem perder
elétrons, o átomo também pode receber elétrons, ocorrendo a quebra de
neutralidade de cargas elétricas.
Nos dois exemplos anteriores, foi
possível verificar que, com a perda ou com o ganho de elétrons, os
átomos deixaram de apresentar carga neutra. Quando isso ocorre, o átomo
recebe uma nova denominação: são chamados de íons.
Os íons
Observe que, se um átomo perder um
elétron, seu numero de prótons fica maior que o número de elétrons.
Assim, o átomo assume uma carga positiva, transformando-se em um íon
positivo, denominado cátion.
Considere novamente o átomo de sódio:
Quando o átomo de sódio perde um elétron,
ele se transforma em um íon de carga positiva (+1). Caso o processo
seja inverso, ou seja, o átomo receba um elétron, o número de elétrons
torna-se superior ao de prótons e o átomo assume uma carga negativa,
transformando-se em íon negativo, denominado ânion.
Agora, observe o átomo de cloro:
Nesse exemplo, a carga do íon cloro passa a valer -1, pois seu átomo de origem recebeu um elétron.
A quantidade de carga de um cátion ou
ânion pode variar de acordo com o número de elétrons que o átomo de
origem perdeu ou recebeu. Assim, é possível verificar a existência de
íons com carga +1, -1, +2, -2, +3, -3 etc.
Veja um exemplo, considerando o átomo de magnésio:
A tabela periódica
Mendeleev e a periodicidade dos elementos
Dmitri Mendeleev foi
professor universitário na Rússia e fez uma importante descoberta na
história da Ciência enquanto estava escrevendo um livro de química.
Ele registrou as propriedades de cada um
dos elementos químicos conhecidos (na época eram 63; hoje são mais de
100) em fichas de papel, cada ficha para um elemento.
Manipulando as fichas, na tentativa de
encadear as idéias antes de escrever uma certa parte da obra, Mendeleev
percebeu algo extraordinário.
Na época, havia evidências científicas de
que os átomos de cada elemento têm massas diferentes. Mendeleev
organizou as fichas de acordo com a ordem crescente da massa dos átomos
de cada elemento. Ele notou que nessa seqüência apareciam, a intervalos
regulares, elementos com propriedades semelhantes. Havia uma
periodicidade, uma repetição, nas propriedades dos elementos.
Entre os muito exemplos de elementos com propriedades semelhantes podemos citar:
- sódio (Na), potássio (K) e rubídio (Rb) –
reagem explosivamente com a água; combinam-se com o cloro e o oxigênio
formando, respectivamente, compostos de fórmulas ECl e E2O (E representa o elemento);
- magnésio (Mg), cálcio (Ca) e estrôncio (Sr)
– reagem com água, mas não tão violentamente; combinam-se com o cloro e
o oxigênio formando, respectivamente, compostos de fórmulas ECl2 e EO.
A tabela periódica de Mendeleev
Com base em sua descoberta,
Mendeleev pôde organizar os elementos em uma tabela, na qual aqueles com
propriedades semelhantes apareciam numa mesma coluna.
Elaborando melhor a sua descoberta, ele
percebeu que pareciam estar faltando alguns elementos para que ela fosse
completa. Mendeleev resolveu, então, deixar alguns locais em branco
nessa tabela, julgando que algum dia alguém descobriria novos elementos
químicos que pudessem ser encaixados nesses locais, com base em suas
propriedades. Ele chegou, até, a prever algumas das propriedades que
esses elementos teriam.
Mendeleev também percebeu que em alguns
locais da tabela seria melhor fazer pequenas inversões na ordem dos
elementos. Em 1871, ele publicou uma versão melhorada de seu trabalho.
Antes de Mendeleev alguns cientistas já
haviam percebido que alguns grupos de elementos tinham propriedades
semelhantes, mas o mérito do químico russo foi o de organizar os
elementos com base em suas propriedades, realizar pequenos ajustes
necessários e deixar locais para elementos que podiam existir, mas que
ainda não haviam sido descobertos.
Os elementos cuja existência foi prevista
por Mendeleev de fato existem na natureza e foram descobertos alguns
anos mais tarde. E as propriedades desses elementos são iguais ou
bastante próximas daquelas previstas por ele.
A tabela periódica atual
Em 1913 e 1914, o inglês Henry Moseley
fez importantes descobertas trabalhando com uma técnica envolvendo raios
X. Ele descobriu uma característica dos átomos que ficou conhecida como
número atômico.
Nesse momento, basta
dizer que cada elemento químico possui um número que lhe é
característico, o número atômico. Quando os elementos químicos são
organizados em ordem crescente de número atômico, ocorre uma
periodicidade nas suas propriedades, ou seja, repetem-se regularmente
elementos com propriedades semelhantes.
Essa regularidade da natureza é conhecida como lei periódica dos elementos.
Outros cientistas aprimoraram as
descobertas de Mendeleev e de Moseley. Esses aprimoramentos conduziram à
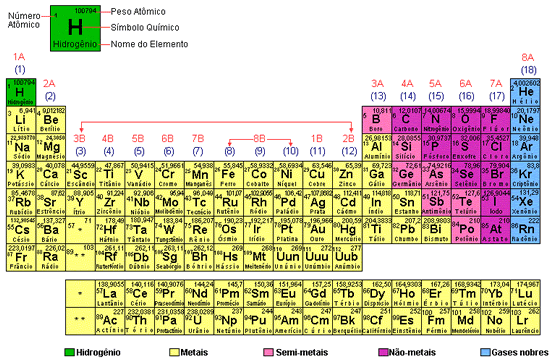
moderna tabela periódica dos elementos, que aparecem na tabela abaixo.
Nela, as linhas horizontais são chamadas de períodos e as colunas (verticais) são denominadas grupos, ou famílias.
A tabela é constituída de períodos e famílias
A simples localização de um elemento
químico na tabela periódica já pode indicar diversas características
específicas desse elemento.
Os períodos
Os elementos são distribuídos na tabela
em ordem crescente da esquerda para a direita em linhas horizontais, de
acordo com o número atômico (Z) de cada elemento, que fica acima de seu símbolo.
Observe a tabela acima. Na tabela há sete linhas horizontais, que são denominadas períodos.
Os períodos indicam o número de camadas
ou níveis eletrônicos que o átomo possui. Por exemplo, o potássio (K)
está localizado no quarto período, e o césio (Cs), no sexto. Isso
significa que na distribuição eletrônica o potássio possui quatro
camadas ou níveis eletrônicos e o césio possui seis.
O paládio (Pd) é uma exceção: apesar de estar na quinta linha horizontal, só possui quatro camadas ou níveis eletrônicos.
Os elementos de um mesmo período possuem o
mesmo número de camadas eletrônicas, que por sua vez é coincidente com o
número do período. Por exemplo:
| Período |
Nº de camadas |
Camadas |
1
|
1
|
K
|
|
|
|
|
|
|
2
|
2
|
K
|
L
|
|
|
|
|
|
3
|
3
|
K
|
L
|
M
|
|
|
|
|
4
|
4
|
K
|
L
|
M
|
N
|
|
|
|
5
|
5
|
K
|
L
|
M
|
N
|
O
|
|
|
6
|
6
|
K
|
L
|
M
|
N
|
O
|
P
|
|
7
|
7
|
K
|
L
|
M
|
N
|
O
|
P
|
Q
|
As famílias
Observe que na tabela periódica existem
18 linhas verticais ou colunas. Elas representam as famílias ou os
grupos de elementos químicos.
Acima das colunas existem números (1, 2, 3 etc.).
Cada coluna representa uma família; por exemplo:
- 1 é a família dos metais alcalinos;
- 2 é a família doa alcalinos terrosos;
- 18 é a família dos gases nobres.
Cada família química agrupa seus
elementos de acordo com a semelhança nas propriedades. Por exemplo, a
família 11 é composta pelos elementos químicos cobre (Cu), prata (Ag) e
ouro (Au). Eles fazem parte do grupo dos metais e apresentam
características comuns: brilho metálico, maleabilidade, ductibilidade,
são bons condutores de calor e de eletricidade.
Assim com esses outros elementos, de uma mesma família possuem semelhanças em suas propriedades.
O número de algumas famílias indica quantos elétrons o elemento químico possui na última camada de sua elétrosfera. Acompanhe a seguir, alguns exemplos.
- O sódio (Na) está na família 1, isto é, possui um elétron na última camada de sua eletrosfera.
- O magnésio (MG) está na família 2, isto é, possui um elétron na última camada de sua elétrosfera.
- O alumínio (Al) encontra-se na
família 3, pois esse elemento possui três elétrons na última camada de
sua elétrosfera.
Família
|
Nº de elétrons na última camada
|
1
|
1
|
2
|
2
|
13
|
3
|
14
|
4
|
15
|
5
|
16
|
6
|
17
|
7
|
18
|
8
|
|
|
Os elementos químicos
situados nas famílias 1 e 2 possuem o número de elétrons na última
camada igual ao número da família a qual pertencem.
Para os das famílias 13 até 18,
obtêm-se o número de elétrons na última camada, subtraindo-se 10 do
número da família. Nas demais famílias essa regra não pode ser aplicada.
O hélio, apesar de estar na família
18, apresenta apenas dois elétrons na última camada, pois esse elemento
possui apenas dois elétrons.
|
| 




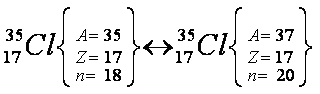
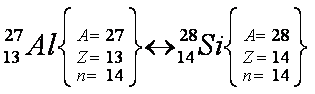
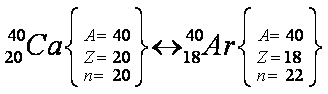





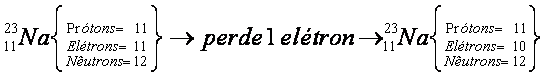

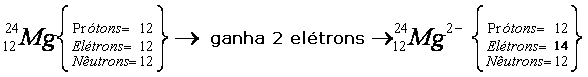








Nenhum comentário:
Postar um comentário